媧擬偲尵偊偽丄乽擬庢傝僔乕僩乿傗乽傕偺偑梟偗傞乿偑巚偄晜偐傇丅
偙偙偱偼乽弮悎側僗僘尦慺傪壛擬偡傞乿傪庢傝忋偘傞丅
僗僘偼乽偼傫偩乿崌嬥偺庡梫尦慺偱偁傞丅
僗僘偼幒壏偱偼屌懱偱偁傝丄232亷偱偼塼懱偵側傞丅
弮悎側僗僘偺0亷偐傜300亷偵偍偗傞帺桼僄僱儖僊乕偲僄儞僞儖僺乕偼
壓恾偺傛偆偵側傞丅丂嵍懁偺帺桼僄僱儖僊乕恾傪尒偰傕戝偒側曄壔偼柍偄丅
塃懁偺僄儞僞儖僺乕恾傪尒傞偲232亷偵偍偄偰戝偒側曄壔偑惗偠偰偄傞丅
232亷偵偍偗傞屌懱偲塼懱偺擬椡妛抣傪妋擣偡傞偲
丂丂丂丂屌懱丂丂丂丂塼懱
G -27.53 -27.53 (kJ/mol)
H 6.00 13.20 (kJ/mol)
S 66.38 80.63 (J/(molK))
偱偁傝丄
斀墳慜(Reactants)偺僄儞僞儖僺乕抣H 偲斀墳屻(Products)偺僄儞僞儖僺乕抣H
傪斾妑偟丄僄儞僞儖僺乕偑憹偊偰偄傟偽丄偦偺暘偺媧擬偑偁傞偙偲
傪堄枴偡傞丅
婰崋G偼帺桼僄僱儖僊乕丄H偼僄儞僞儖僺乕丄S偼僄儞僩儘僺乕傪帵偡丅
丂Sn(屌懱) + 媧擬 --> Sn(塼懱乯
丂媧擬検偼 7.2 (kJ/mol) 偲側傞丅梈夝擬偵憡摉偡傞丅
偙偙偱偼乽232亷枹枮偺忬懺偐傜丄壛擬偟丄232亷偺忬懺傊乿偲偟偨偑丄帇揰傪曄偊偰傒傛偆丅
偨偲偊偽揝(Fe)偺応崌乽231亷偺揝屌懱傪丄232亷偺娐嫬偵抲偄偨乿偲偟偰傕戝偒側曄壔偼婲偒側偄丅
偟偐偟丄僗僘(Sn)偺応崌乽231亷偺僗僘屌懱傪丄232亷偺娐嫬偵抲偄偨乿偲偡傟偽媧擬偲側傞丅
丂丂丂丂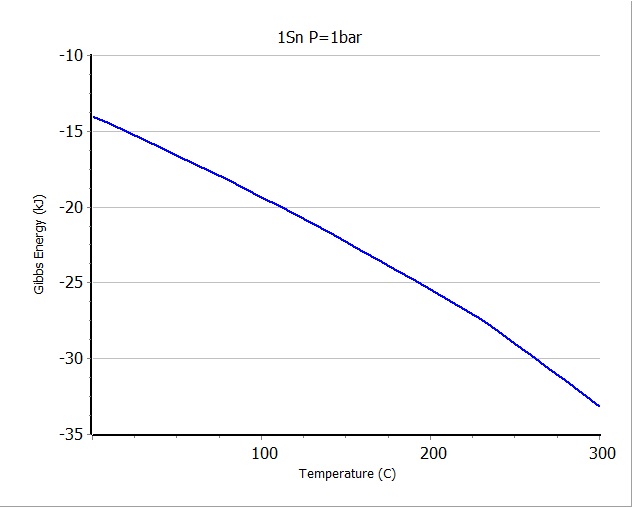 丂丂丂丂
丂丂丂丂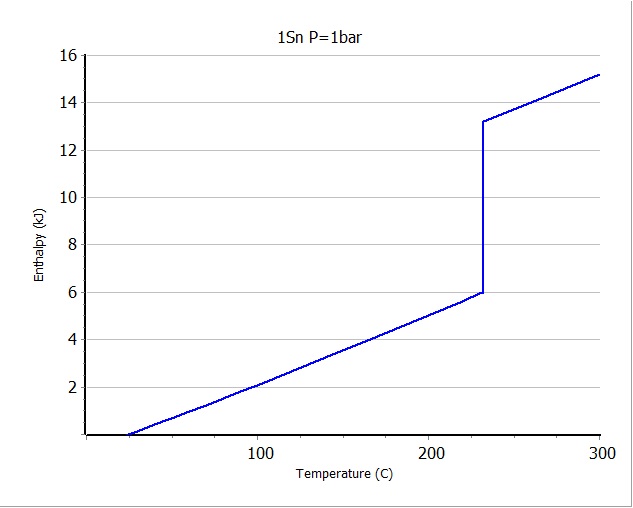 丂栠傞
丂栠傞
Copyright(C) 2017 Materials Design Technology Co., Ltd. All Rights Reserved.
 丂丂丂丂
丂丂丂丂 丂栠傞
丂栠傞
丂丂丂丂
丂栠傞